
Дихлорэтан
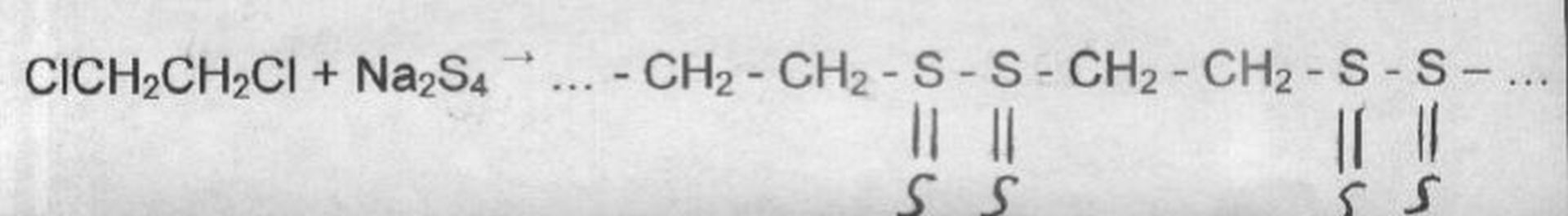
Тиокол
Дихлорэтан (1, 2-дихлорэтан, хлористый этилен) ClCH2CH2Cl представляет собой бесцветную жидкость с запахом, напоминающим хлороформ. Температура плавления –35, 7°C, температура кипения 83, 483°С при 760 мм рт. ст., 20°С при 63 мм рт. ст., плотность 1, 253 г/см3. Теплота испарения (при температуре кипения) 7, 654 ккал/моль, теплота плавления 2, 112 ккал/моль, теплоёмкость 30, 86 ккал/моль (26, 72°). Электропроводность 3 . 10-10 ом . см-1 (25°), диэлектрическая проницаемость 10, 36 (25°). Растворимость в воде составляет 0, 81 вес. % (при 20°), растворимость воды в дихлорэтане 0, 15 вес. % (при 20°). Азеотропная смесь с водой содержит 82, 9 вес. % дихлорэтана; температура кипения 71, 5°С.
Дихлорэтан получают взаимодействием хлора и этилена:
CH2 = CH2 + Cl2 → ClCH2CH2Cl.
Побочно получаются полихлорэтаны, главным образом трихлорэтан.
При нагревании с водой, раствором соды или суспензией гашёной извести, дихлорэтан образует этиленгликоль; действием щёлочи или пиролизом превращается в хлористый винил. При нагревании дихлорэтана с аммиаком под давлением даёт этилендиамин, с цианистым натрием дихлорэтан образует динитрил янтарной кислоты. При нагревании с растворами полисульфидов натрия дихлорэтан образует каучукоподобное вещество тиокол.
Дихлорэтан — сильное наркотическое средство, при приёме внутрь или вдыхании паров вызывает отравление. Допустимая концентрация паров в воздухе производственных помещений 0, 01%. Дихлорэтан мало огнеопасен. Пределы взрывчатости в воздухе 6, 20 — 15, 90 об. %.
Дихлорэтан широко применяется в качестве растворителя (в экстракционных процессах, при очистке текстильных материалов, в лакокрасочной промышленности), как составная часть антидетонаторных смесей, в качестве фумиганта, как азеотропная добавка при дистилляции, а также как сырьё в производстве тиоколов и других. В быту часто используется как клей для пластмасс и оргстекла.