
Литий-ионный аккумулятор
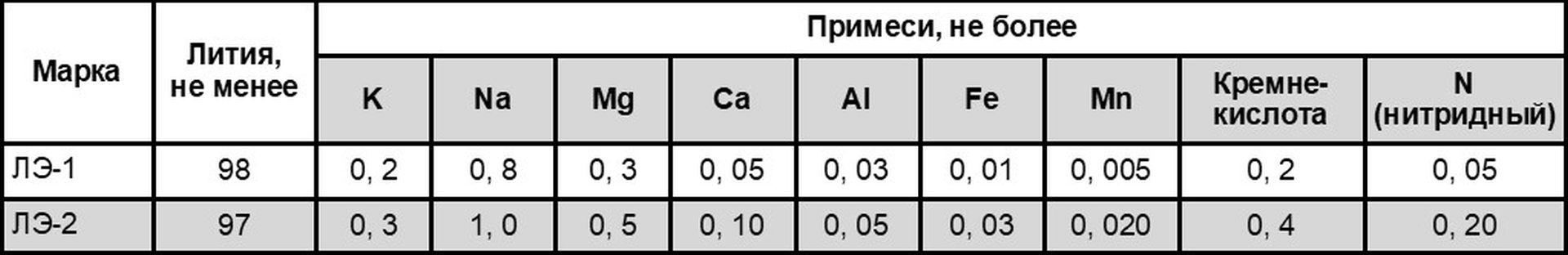
Марки и химический состав лития
Литий - химический элемент, символ Li (лат. lithium, от греч. Lithos — камень. Металл впервые был обнаружен в твёрдом минерале). Имеет порядковый номер 3, атомный вес 6, 939, плотность 0, 53 г/см3, температуру плавления 180°С, температуру кипения 1350°С.
Литий — щелочной металл серебристо-белого цвета. Он открыт в 1817 г. Литий после водорода и гелия имеет наименьшую атомную массу, наименьшую среди всех металлов плотность (0, 534 при 20 градусах, 0, 507 в расплавленном состоянии и 0, 441 при 1000°С) и наибольшую теплоёмкость. Он почти в два раза легче воды, в 5 раз легче алюминия, в 15 — железа, в 20 — свинца и в 40 раз легче осмия.
По сравнению с другими щелочными металлами литий обладает большей химической стойкостью. На воздухе при комнатной температуре он медленно корродирует с образованием смеси нитрида и окиси лития, поэтому его хранят в закрытых сосудах или в инертной среде.
Литий активно реагирует с водородом, азотом, окислами и сульфидами, растворёнными в металлах, находящихся в расплавленном состоянии, образуя легко всплывающие нерастворимые химические соединения. Благодаря этим свойствам литий успешно применяют в качестве раскислителя и дегазатора многих металлов. Под влиянием лития практически устраняется пористость меди, возрастает её плотность и электропроводность. Литий улучшает свойства алюминиевоцинковых сплавов — повышает их прочность и коррозионную стойкость. Он улучшает также технологические свойства чугуна и повышает его прочность.
Со многими металлами литий образует соединения, обладающие высокой температурой плавления и большой твёрдостью. Эти свойства позволяют применять литий в качестве компонента лёгких и антифрикционных сплавов.
Хорошими механическими свойствами и высокой коррозионной стойкостью обладают легкие магнийлитиевые и магнийлитиево-алюминиевые сплавы. Высокими механическими свойствами и высокой коррозионной стойкостью обладают сверхлёгкие сплавы лития с бериллием.
Литий применяют как катализатор при производстве синтетического каучука.
Благодаря высокой теплоёмкости и теплопроводности, широкому температурному интервалу жидкого состояния, малой вязкости и плотности жидкий литий очень эффективно может быть использован в качестве теплоносителя в урановых реакторах при производстве атомной энергии.
Окись лития является составной частью стёкол с низким коэффициентом теплового расширения, способных пропускать ультрафиолетовые лучи. Гидроокись лития входит в состав электролита щелочных аккумуляторов. LiOH повышает их ёмкость на 20%, расширяет рабочий температурный диапазон и в 2 раза увеличивает срок службы. В последнее время большое распространение получили литий-ионные и литий-полимерные аккумуляторы. Соли лития используют в пиротехнике, в сварочных флюсах, в химической промышленности и в медицине.
Соединение лития с водородом — гидрид лития — представляет собой твёрдую губчатую массу. Смазки, в которых имеется литиевое мыло, сохраняют свои свойства в широком диапазоне температур, что важно для высотной авиации, а также для работы деталей в северных и южных районах. Соли лития входят в состав оптических стёкол, увеличивая их прозрачность.
При горении в кислороде литий выделяет большое количество тепла, что может быть использовано в ракетных двигателях. Соединения лития активно разлагают углекислоту и их применяют для очистки воздуха в подводных лодках при длительном их погружении.
Изотоп лития Li6 является практически единственным источником для производства тяжёлого водорода — трития (Н3), играющего важную роль в термоядерных реакциях.
Марки и химический состав лития приведены в таблице (по ГОСТ 8774-58, СССР).